Molekularno-kinetička teorija omogućava da se, analizom mikroskopskog ponašanja sistema i upotrebom metoda statističke mehanike, dobiju važne makroskopske karakteristike termodinamičkog sistema. Jedna od mikroskopskih karakteristika, koja je povezana sa temperaturom sistema, je srednja kvadratna brzina molekula gasa. Dajemo formulu za to i razmatramo je u članku.
Idealni plin
Odmah napominjemo da će formula za kvadratnu prosječnu brzinu molekula plina biti data posebno za idealni plin. Pod njim se u fizici smatra takav sistem sa više čestica u kojem čestice (atomi, molekuli) ne interaguju jedna s drugom (njihova kinetička energija premašuje potencijalnu energiju interakcije za nekoliko redova veličine) i nemaju dimenzije, to jest, to su tačke sa konačnom masom (udaljenost između čestica nekoliko redova veličine veća od njihove veličine.linearni).
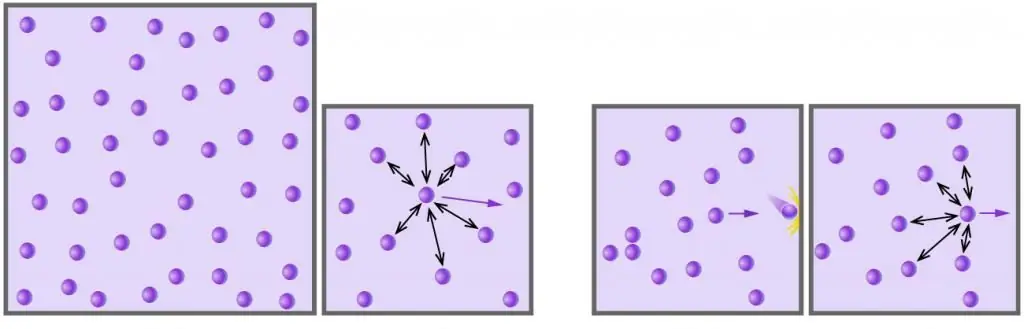
Svaki gas koji se sastoji od hemijski neutralnih molekula ili atoma, a koji je pod niskim pritiskom i ima visoku temperaturu, može se smatrati idealnim. Na primjer, zrak je idealan plin, ali vodena para više nije takva (između molekula vode djeluju jake vodikove veze).
Teorija molekularne kinetike (MKT)

Proučavajući idealan gas u okviru MKT-a, treba obratiti pažnju na dva važna procesa:
- Plin stvara pritisak prenoseći na zidove posude koja ga sadrži, moment kada se molekuli i atomi sudaraju sa njima. Takvi sudari su savršeno elastični.
- Molekuli i atomi plina kreću se nasumično u svim smjerovima s različitim brzinama, čija distribucija odgovara Maxwell-Boltzmannovoj statistici. Vjerovatnoća sudara između čestica je izuzetno mala, zbog njihove zanemarljive veličine i velikih udaljenosti između njih.
Uprkos činjenici da su pojedinačne brzine čestica gasa veoma različite jedna od druge, prosečna vrednost ove vrednosti ostaje konstantna tokom vremena ako nema spoljašnjih uticaja na sistem. Formula za srednju kvadratnu brzinu molekula gasa može se dobiti razmatranjem odnosa između kinetičke energije i temperature. Mi ćemo se pozabaviti ovim pitanjem u sljedećem pasusu članka.
Izvođenje formule za kvadratnu prosječnu brzinu molekula idealnog plina
Svaki student zna iz opšteg kursa fizike da se kinetička energija translacionog kretanja tela mase m izračunava na sledeći način:
Ek=mv2/2
Gdje je v linearna brzina. S druge strane, kinetička energija čestice se također može odrediti u smislu apsolutne temperature T, koristeći faktor konverzije kB (Boltzmannova konstanta). Pošto je naš prostor trodimenzionalan, Ek se izračunava na sljedeći način:
Ek=3/2kBT.
Ekvivalentno obema jednakostima i izražavajući v iz njih, dobijamo formulu za prosečnu brzinu kvadratnog idealnog gasa:
mv2/2=3/2kBT=>
v=√(3kBT/m).
U ovoj formuli, m - je masa čestice gasa. Njegova vrijednost je nezgodna za korištenje u praktičnim proračunima, jer je mala (≈ 10-27kg). Da bismo izbjegli ovu neugodnost, prisjetimo se univerzalne plinske konstante R i molarne mase M. Konstanta R sa kB povezana je jednakošću:
kB=R/NA.
Vrijednost M je definirana na sljedeći način:
M=mNA.
Uzimajući u obzir obje jednakosti, dobijamo sljedeći izraz za srednju kvadratnu brzinu molekula:
v=√(3RT/M).
Dakle, srednja kvadratna brzina čestica gasa je direktno proporcionalna kvadratnom korenu apsolutne temperature i obrnuto proporcionalna kvadratnom korenu molarne mase.
Primjer rješavanja problema
Svi znaju da je vazduh koji udišemo 99% azota i kiseonika. Potrebno je odrediti razlike u prosječnim brzinama molekula N2 i O2 na temperaturi od 15 o C.

Ovaj problem će biti riješen uzastopno. Prvo, prevedemo temperaturu u apsolutne jedinice, imamo:
T=273, 15 + 15=288, 15 K.
Sada napišite molarne mase za svaki molekul koji se razmatra:
MN2=0,028 kg/mol;
MO2=0,032 kg/mol.
Budući da se vrijednosti molarnih masa neznatno razlikuju, njihove prosječne brzine na istoj temperaturi bi također trebale biti bliske. Koristeći formulu za v, dobijamo sljedeće vrijednosti za molekule dušika i kisika:
v (N2)=√(38, 314288, 15/0, 028)=506,6 m/s;
v (O2)=√(38, 314288, 15/0, 032)=473,9 m/s.
Budući da su molekuli dušika nešto lakši od molekula kisika, kreću se brže. Prosječna razlika u brzini je:
v (N2) - v (O2)=506,6 - 473,9=32,7 m/s.
Rezultirajuća vrijednost je samo 6,5% prosječne brzine molekula dušika. Skrećemo pažnju na velike brzine molekula u gasovima, čak i na niskim temperaturama.






